医療機関向け治験ソリューション
DDworks Trial Site

これまで一般的に紙で管理が行われてきた治験関連文書、紙による運用においては、関係者間でのやりとりや保管業務、IRBに関連する業務などに多大な時間と労力を要し、また、大量に発生する書類の保管場所の枯渇も深刻な問題となっておりました。DDworks Trial Siteは、医療機関における治験文書およびそれに関係するプロセスを電子化することで、大幅な業務の効率化と、品質の向上を同時に実現します。
医療機関の治験DX
-
文書に関連する業務の集約治験依頼者との文書のやり取り、院内の文書の承認ワークフロー、IRBの審査資料のとりまとめ、審査結果通知書の発行など、医療機関における文書に関連する業務をDDworks Trial Siteに集約することができます。
-
業務の効率化書式の一括作成機能や、審査関係の操作を一括で処理できる機能、各種状況を可視化できる一覧帳票等により、治験関連文書に関する業務を効率よく行えるようになります。
-
プロセス管理による業務品質向上治験関連文書に関する業務プロセスを支援する機能も備えており、システムを利用することで同時に業務品質を向上させることができます。
安心してご利用いただける運用実績
-
 高い利用実績日本国内で治験を実施する医療機関のうち約41%(注1)での利用実績があります。また、DDworks Trial Site を通じて約400社の製薬企業、CRO(注2)の皆さまにご利用いただいております。
高い利用実績日本国内で治験を実施する医療機関のうち約41%(注1)での利用実績があります。また、DDworks Trial Site を通じて約400社の製薬企業、CRO(注2)の皆さまにご利用いただいております。 -
 87%の業務効率化紙からDDworks Trial Site に運用を切り替えたことで、87%の業務時間削減を実現。加えて、書類作成や保管に関するミスを減少し、治験の現場での効率化と品質向上を同時に実現します。
87%の業務効率化紙からDDworks Trial Site に運用を切り替えたことで、87%の業務時間削減を実現。加えて、書類作成や保管に関するミスを減少し、治験の現場での効率化と品質向上を同時に実現します。 -
 最短3か月で稼働治験文書関連業務において、富士通がご提供する標準化された業務手順に沿って運用いただくことで、コストを抑えて3ヶ月での早期稼働が可能です。(注3)
最短3か月で稼働治験文書関連業務において、富士通がご提供する標準化された業務手順に沿って運用いただくことで、コストを抑えて3ヶ月での早期稼働が可能です。(注3) -
 強力なサポートシステム選定から導入、稼働後までトータルでサポート。導入時のプロジェクトマネジメントはもちろん、稼働後はサポートデスクに加え、施設担当のスペシャリストがあらゆるお問合せにシームレスに対応します。
強力なサポートシステム選定から導入、稼働後までトータルでサポート。導入時のプロジェクトマネジメントはもちろん、稼働後はサポートデスクに加え、施設担当のスペシャリストがあらゆるお問合せにシームレスに対応します。
- (注1)2024年7月30日時点 富士通調べ:SMO経由でのDDworks Trial Site の利用および電磁化SOP設置を含む826施設を基に算出
- (注2)治験国内管理人含む
- (注3)施設の現行の運用に合わせて、富士通が全面的にご支援してシステムの業務手順をしっかり作り込む導入プラン(6ヵ月)もご用意しております。
日本の医療機関の治験プロセスに最適化された
DDworks Trial Site
DDworks Trial Site を導入したユーザー様からは、「紙の運用からスムーズに電子に移行することができた」と評価をいただいております。DDworks Trial Siteは製品開発の段階において、治験に関わる多様なステークホルダーの方の利便性を向上できることを目的として、モデルユーザー様との実証実験を行いました。
システム運用イメージ
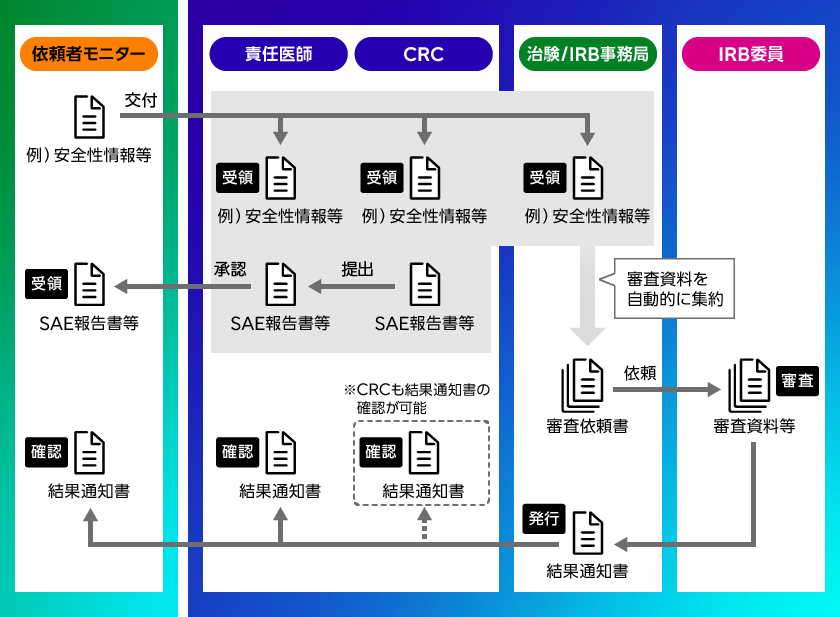
- 依頼者と施設の間で、双方向の文書の電子授受
- 依頼者とのQ&A管理(GCP省令第41条ガイダンス第1項として利用可能)
- 院内の関係者での文書の電子レビュー/承認(例:CRC⇒責任医師、事務局⇒院長)
- ユーザIDとパスワードによる電子署名が可能
- SAEの一元管理、報告書の作成補助
- 追加報作成のためのWORDファイルの保管も可能
- 逸脱情報の一元管理、書式の自動作成が可能(重大、緊急回避、それ以外)
- 全試験の逸脱情報を取りまとめて分類、評価が可能
- 審査依頼の一括電子受付、書式4自動作成
- 審議資料の事前レビュー、依頼者問合せの電子化
- 書式5の一括作成/通知、会議の記録の概要の作成補助
- 治験文書をインターネットのクラウド上で管理
- 電子ファイル、スキャンした紙ファイルの両方に対応
一日も早く必要な患者に新薬を届けるために
医療機関の治験プロセスを最適化するDDworks Trial Site は、今後も定期的なレベルアップを行い、機能追加や最新の規制に対応し、また、新しいトレンドにも追従していきます。そうすることで、医療機関の治験プロセスをより持続可能にし、さらに、医薬・医療連携を加速することで、一日も早く必要な患者に新薬を届けることが可能になります。
ご不明な点やご要望などございましたら、
お気軽に下記お問い合わせフォームよりお問い合わせください。
Virtual Pharmaに関するお問い合わせ・ご相談
当社はセキュリティ保護の観点からSSL技術を使用しております。
